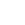Un mosquito resistente: la evolución del vector de la malaria en Sudamérica frente a los insecticidas
Publicado el
Por Francisco Vidal
Son las cinco de la tarde en una comunidad a orillas del río Amazonas, en Loreto. Los jóvenes no piensan en los mosquitos, están jugando fútbol y el partido no terminará antes de las seis. Después vendrá el baño en el río, cuando el sol haya bajado lo suficiente para que el calor sea soportable. Es exactamente en ese intervalo, entre el atardecer y la oscuridad, cuando el mosquito Anopheles darlingi empieza su propio turno. El biólogo Freddy Álava lleva veinticinco años observando las consecuencias de aquel momento en el que el cuerpo queda al descubierto, mientras la nube de mosquitos se aproxima a su objetivo.
Como experto en vigilancia vectorial y responsable de la Sala Situacional Epidemiológica de la Gerencia Regional de Salud (GERESA) de Loreto, Freddy trabaja identificando dónde se reproducen los vectores, cómo se comportan y qué cambios podrían volver más difícil controlarlos. “Si no conocemos cómo se comporta el mosquito en cada lugar, nuestras intervenciones pueden perder efectividad”, explica. En el Perú, más del 90% de los casos de malaria se registran en la Amazonía, principalmente en Loreto. Allí, factores como la humedad y el aumento del río crean las condiciones ideales para la proliferación del mosquito.
Durante mucho tiempo, las estrategias para combatir la malaria se han concentrado en el diagnóstico temprano, el tratamiento oportuno y el control del mosquito mediante insecticidas, pero existen otros factores cruciales en la lucha contra la enfermedad. Una reciente investigación internacional publicada en Science y en la que participó la Dra. Dionicia Gamboa, investigadora y profesora principal de la Facultad de Ciencias e Ingeniería de Cayetano Heredia, revela que el Anopheles darlingi, principal mosquito transmisor de malaria en la región, posee una enorme diversidad genética y ya muestra señales de adaptación a los insecticidas usados para combatirlo.

La enfermedad que no cede
La Amazonía peruana tiene su propio calendario de la malaria. Cuando los ríos crecen en la temporada de creciente, los criaderos naturales del vector se multiplican y con ellas el riesgo de transmisión. Cuando bajan las aguas, en la vaciante, los criaderos disminuyen y los casos parecen controlarse. Pero nunca desaparecen del todo. Según el Centro Nacional de Epidemiología, Prevención y Control de Enfermedades (CDC) del Ministerio de Salud, hasta abril de este año el Perú acumulaba 6671 casos de malaria, con Loreto y Junín concentrando el 99,8% del total. Casi la mitad de los afectados, el 48,4%, son niños menores de 12 años.
Por su parte, la Organización Mundial de la Salud señala que Perú logró reducir sus casos en un 49% entre 2015 y 2024, pero también advierte que entre 2023 y 2024 se registró un repunte significativo, impulsado por movimientos migratorios, la expansión de la minería aurífera y los efectos del fenómeno de El Niño sobre los ecosistemas amazónicos. Para el Dr. César Munayco Escate, epidemiólogo y director del CDC, la respuesta a esa persistencia requiere hoy herramientas que van más allá del conteo de casos:

«La vigilancia epidemiológica nos va a ayudar a identificar cuáles son los riesgos y las zonas donde hay mayor incidencia. Con el uso de modelamiento matemático y otras técnicas de inteligencia artificial, se puede predecir inclusive dónde pueden aparecer los brotes de malaria. En países con realidades tan diversas, resulta clave fortalecer la vigilancia para tener evidencia necesaria para abordar este problema de salud».
En un contexto en que el propio mosquito está cambiando, esa capacidad de anticipación resulta esencial. Durante décadas, los grandes estudios de genómica de vectores maláricos se habían concentrado en África y Asia, donde el conocimiento acumulado ha permitido anticipar resistencias y diseñar intervenciones específicas. Pero el linaje del An. darlingi se separó del de su pariente africano, An. gambiae, hace aproximadamente 90 millones de años, cuando los dinosaurios aún habitaban la Tierra. Lo que se sabe del mosquito africano no es directamente transferible a la Amazonía y, sin embargo, era prácticamente lo único con lo que se contaba.

Un mapa genético sin precedentes
La investigación en la que participó la Dra. Gamboa presenta el primer análisis genómico poblacional a gran escala de este mosquito. El equipo internacional, liderado por el Dr. Jacob A. Tennessen de la Escuela de Salud Pública T.H. Chan de Harvard, secuenció el genoma completo de 1094 hembras adultas de An. darlingi en 16 localidades de seis países sudamericanos: Brasil, Perú, Venezuela, Colombia, Guyana y Guayana Francesa.
Los resultados señalan que el An. darlingi posee una diversidad genética extraordinaria. En la mayoría de los individuos, más del 2% de las bases del ADN difieren entre sí, un nivel comparable al del complejo An. gambiae, el principal transmisor africano reconocido como caso emblemático de alta variabilidad genética. En términos prácticos, esa variabilidad le otorga al mosquito sudamericano una capacidad mayor para adaptarse a nuevas presiones, incluidos los insecticidas.
El análisis reveló además que las poblaciones de An. darlingi en Sudamérica no forman una sola comunidad conectada. Genéticamente, se agrupan en tres grandes clústeres bien diferenciados: el amazónico-atlántico, el del Orinoco y el del Chocó, al oeste de los Andes. La distancia genética entre estos grupos es tan marcada que supera incluso la que existe entre distintas especies de mosquitos africanos que conviven en su mismo continente. Lo que las separa no son los grandes ríos, como se pensaba, sino los límites entre cuencas hidrográficas. El mosquito depende del agua para reproducirse, y los ríos, con toda la actividad humana que los acompaña, pueden ser vías de dispersión más que de separación.
El estudio también descartó la existencia de especies crípticas en An. darlingi. Es decir, no encontró mosquitos físicamente idénticos que, en realidad, pertenezcan a linajes genéticamente distintos y no se reproduzcan entre sí. En África, la existencia de este fenómeno dificultó durante décadas las estrategias de control, porque muchas intervenciones se diseñaban pensando en un solo mosquito cuando en realidad coexistían varios. En Sudamérica, en cambio, los resultados sugieren que las poblaciones locales de An. darlingi son genéticamente homogéneas. Esto podría facilitar el diseño de estrategias de control adaptadas a cada territorio.

Resistencia y adaptación confirmada por los genes
El hallazgo más relevante para la salud pública de la Amazonía se basa en señales de selección positiva en el genoma del mosquito. Es decir, indicios de que ciertas variantes genéticas se están volviendo más comunes porque le otorgan ventajas para sobrevivir bajo determinadas presiones ambientales, como el uso de insecticidas. Con el tiempo, esas variantes pueden extenderse en la población. Una de las señales más fuertes detectadas en el estudio apareció precisamente en Loreto. Allí se registraron los resultados estadísticos particularmente consistentes en distintas pruebas independientes. No es un dato menor, pues también es una de las zonas con mayor actividad agrícola entre los lugares analizados.
Uno de los genes más claramente asociados a estas señales de adaptación fue CYP6AA1, vinculado en otros mosquitos con resistencia a insecticidas del tipo piretroide. Freddy Álava pudo observar ese fenómeno en campo antes de que los genomas ofrecieran una explicación. “Loreto dejó de usar piretroides en 2018; observamos resistencia de los vectores a esa molécula luego de 12 años de uso”, recuerda. A partir de entonces, la GERESA de Loreto adoptó el organofosforado Pirimiphos methyl. El estudio genómico, publicado ahora, ayuda a entender los mecanismos asociados a esa resistencia.

A diferencia de otras especies, donde ciertas mutaciones bloquean el efecto del insecticida en el sistema nervioso, los resultados en Anopheles darlingi apuntan a mecanismos metabólicos vinculados con la detoxificación de estas sustancias. Según el estudio, esta adaptación puede surgir de forma paralela en distintas poblaciones y sobre fondos genéticos diferentes, sin necesidad de expandirse desde un único punto de origen.
Eso significa que, incluso sin dispersión entre regiones, la resistencia podría emerger nuevamente en distintos lugares. Los investigadores plantean, además, que esta presión evolutiva podría venir no solo de los insecticidas de control vectorial, sino también de agroquímicos que llegan a los cuerpos de agua donde el mosquito se reproduce. En ese escenario, la biología molecular cobra especial relevancia. “El mayor riesgo de enfrentar la malaria sin entender cómo evoluciona el mosquito que la transmite es implementar estrategias poco efectivas mientras el riesgo de brotes aumenta”, señala Luis Esteban Cabrera Sosa, biólogo egresado de Cayetano Heredia.

Para convertir esa evidencia genómica en política pública, el camino sigue siendo largo. El Dr. Jaime Chang Neyra, médico con 27 años gestionando iniciativas de cooperación técnica en malaria en once países de América Latina, señala que la clave está en evolucionar al ritmo que evoluciona el contexto y adoptar las nuevas medidas con celeridad y continuidad:

«Hoy en día vemos herramientas modernas y relativamente nuevas, como las que están soportadas por la biología molecular, que tenemos que incorporar a la vigilancia de la malaria. La experiencia nos demuestra que nos hemos demorado hasta siete años para empezar a aplicar una pieza de conocimiento nuevo. Cuando hacemos proyectos de tres o cinco años, corremos el riesgo de no llegar a ese nivel de cambio institucional».
La batalla donde el comportamiento es protagonista
Volviendo a aquella comunidad loretana al atardecer, algunos de los jóvenes que entraron a bañarse al río retornan a sus casas con picaduras, pero no es algo nuevo. “Cuando hacemos encuestas en poblaciones, las personas responden que tuvieron malaria diez, quince, veinte veces», recuerda Freddy. “Al convivir tanto tiempo con la enfermedad, muchos ya reconocen sus síntomas antes de acudir a un establecimiento de salud. El problema resulta cuando se acercan una semana después y, en ese intervalo, el ciclo de transmisión continúa en la comunidad”.
La Dra. Elisa Vidal Cárdenas, representante regional sénior para América Latina en Medicines for Malaria Venture (MMV), subraya que la lógica de trabajo con las comunidades debe estar presente desde el diseño mismo de cualquier intervención:

«Es importante involucrar a los actores y beneficiarios desde el inicio, y con beneficiarios no me refiero solo al sistema de salud. Incorporar a las personas afligidas por enfermedades como la malaria en el diseño y en las tomas de decisiones genera una apropiación de las tecnologías de salud que se van a implementar. La data tiene que traducirse para una mayor comprensión de cómo estas innovaciones les van a servir de diferentes formas».
Para los especialistas, la dimensión educativa no es complementaria al control vectorial, sino parte de su condición. «Venimos muchos años enseñando cuáles son las medidas preventivas para la malaria, como dormir bajo mosquitero, usar ropa protectora, bañarse antes que anochezca, acudir inmediatamente al establecimiento de salud si tiene síntomas», enumera Freddy. Si bien las limitaciones de acceso a la salud suponen una barrera crucial para cualquier enfermedad endémica, el rol de la comunidad también resulta esencial para hacerles frente.
La noche ha caído sobre el río y el An. darlingi, mientras tanto, continúa su vuelo entre la vegetación, como lo ha hecho durante millones de años. La diferencia es que ahora la ciencia en Sudamérica tiene su mapa genético completo. Bajo una respuesta que integre esfuerzos científicos, institucionales y comunitarios, podríamos enfrentar la enfermedad de manera más efectiva y, por primera vez, a la misma velocidad con la que el mosquito se adapta.

Conoce más sobre la investigación en el artículo “Population genomics of Anopheles darlingi, the principal South American malaria vector mosquito”.
Puedes leer la infografía con los hallazgos científicos dando click aquí.
Investigadora herediana participante en el artículo científico:

Dra. Dionicia Gamboa.